构建人工细胞的两种主要方法是自上而下和自下而上。自上而下方法通过生物技术移除活细胞中的非必要基因和细胞器,最终得到具备最小生存功能的细胞。
而自下而上方法则从简单的非生命物质开始,逐步构建具备细胞功能的仿生结构,避免了细胞的复杂性。
通常使用类似细胞膜的材料模拟内外环境的分隔,并在内部组装细胞器等结构,模仿生物细胞的核心组成部分。通过引入酶、基因等活性物质,支持生化反应,赋予这些区室特定的功能。
在芯片设计的微环境中,可以组装出具备生长、自主活动和自我复制能力的微结构系统,进行高度受控的生化反应。这种技术的发展将大大推动人工细胞研究,并在自下而上合成生物学的未来发展中发挥关键作用。
1. 人工细胞的主要分类
人工细胞的内部和外部由一层屏障隔开,功能类似于生物细胞膜。形成屏障时可生成多种结构类型,如微囊泡、凝聚物和微液滴,成为人工细胞分类的依据之一。
其中,双层膜包裹水核形成的微囊泡与生物细胞形态最为接近,且是常见类型。脂质膜因其优良的生物相容性和与细胞膜的相似性备受关注。其主要构成单元——磷脂,拥有亲水头和疏水尾,在水中能自发组装成脂质体(liposomes)。
脂质体由于与天然生物膜的相似性以及与膜蛋白的兼容性,成为人工细胞构建的“金标准”。根据大小和双层膜数量,脂质体分为小单层脂质体(SUVs,<100nm)、大单层脂质体(LUVs,100-1000nm)、巨型单层脂质体(GUVs,>1μm)和多层脂质体(MLVs)。
其中,GUVs与细胞大小相当,是人工细胞的常用基础结构。然而,脂质体膜缺少蛋白质和糖类,也没有细胞骨架的支撑。
相比之下,聚合物囊泡具有更好的机械性能和稳定性,能更好地抵抗外部环境变化,且具备更高的强度和寿命,能够有效保护内部物质。
其组成单元嵌段共聚物还可以根据需求定制其理化性质。然而,聚合物囊泡不适合膜蛋白或分子通道的嵌入。
为结合脂质体和聚合物囊泡的优势,出现了脂质/聚合物混合囊泡。这类囊泡兼具脂质体的生物相容性和聚合物的结构稳定性,其理化性质可以灵活调整,以适应不同应用需求。
微流控技术的进步加速了液滴技术的应用。与细胞大小相当的油包水(W/O)微液滴在人工细胞构建中广泛使用。
这类液滴内部环境与天然细胞相似,为保持稳定性,通常用磷脂或人工表面活性剂包裹。由于油水界面的高界面张力,微液滴展现出更强的稳定性和操作性。
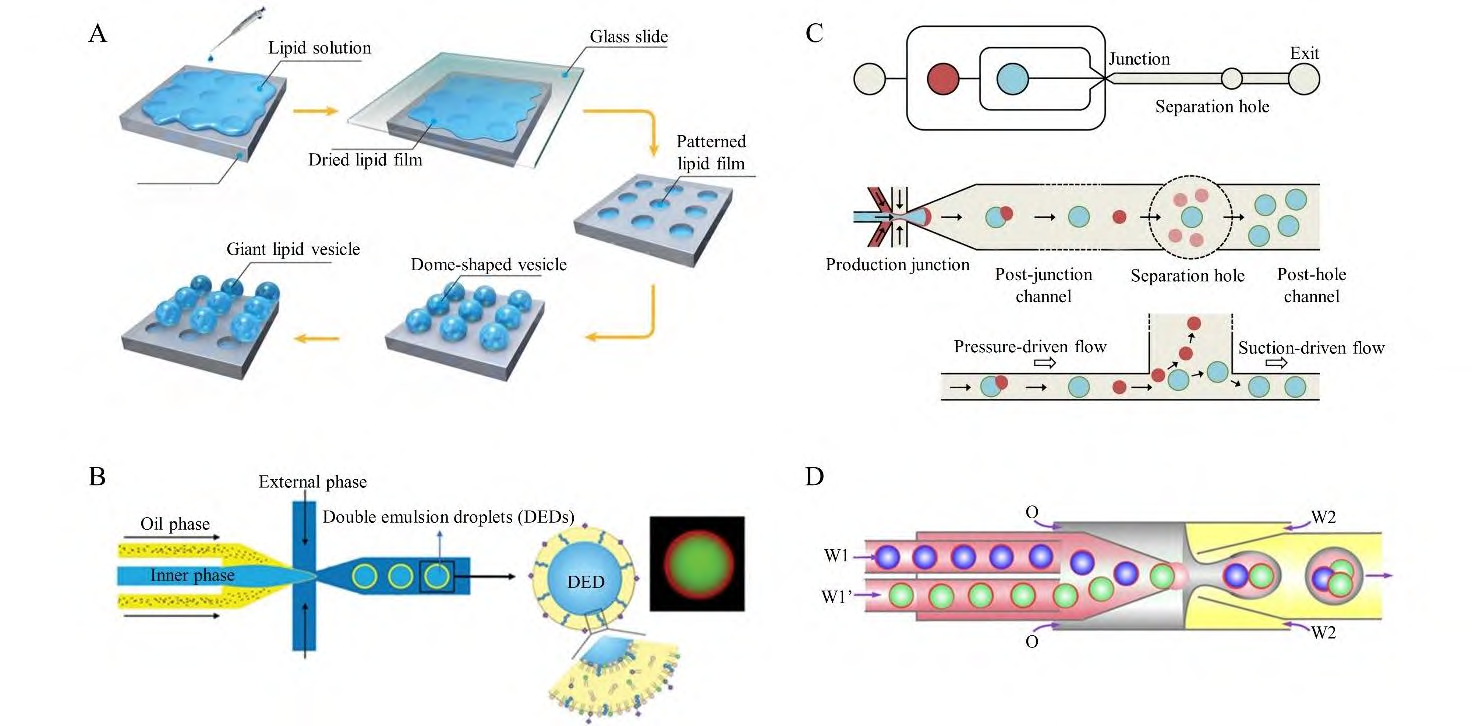
2. 微流控芯片上人工细胞的构建
1) 囊泡结构的制备
基于两性分子构建脂质体囊泡的方法主要有两类。
第一类方法是先制备脂双层膜,再按一定规律卷曲形成封闭囊泡,包裹水相内容物。首先在固体表面涂布有机溶剂,形成层状磷脂干膜,随后加入水溶液,使磷脂分子水合,生成巨型囊泡。
这种方法操作简单、高效,但GUVs的尺寸不均匀,膜结构难以控制,还会产生多层副产物,且装载效率较低。
第二类方法基于乳液技术,在油相中生成的水相液滴通过油/水界面包裹单层脂膜。通过相转移等手段,去除液滴周围的油相,同时形成另一层脂膜,最终构建出双层膜的脂质体。
该方法先形成结构和尺寸高度一致的单层膜囊泡,再通过相转移构建双层膜,过程可利用不同微流控模块独立完成。
目前,常用的液滴微流控策略包括水/油/水(W/O/W)双乳液法,在微流控芯片上通过大液滴封装小液滴,连续生成双乳液囊泡。最内层水相包裹亲水分子,脂质体的两亲分子溶解在油相中,形成稳定的W/O/W乳液后,再去除油相。
此外,液滴裂变、介电泳力和电润湿力等技术也被应用于构建基于液滴的人工细胞结构。
随着微加工和微流控技术的快速进步,创新的制备方法不断涌现,如利用3D打印技术构建人工细胞,这种方法产率高、难度较低,但囊泡尺寸较大,且不易形成复杂的内部结构。
2) 胞内区室化构建
区室化是生物学中的重要组织原则,能够实现复杂而明确的空间和功能划分,允许不同的化学环境共存,建立化学梯度,维持非平衡状态,并隔离不兼容的成分。
为了构建更接近生物特性的人工细胞,通常通过自组装形成区室化结构。微流控技术能够对自组装过程进行精确控制,从而实现区室结构的逐一组装。通过生成多层或多囊泡的脂质体,可以构建多区室结构。
液滴微流控技术能够有效控制多区室囊泡,精准定义区室的数量、大小及其脂质组成和内部内容。此外,还可以通过功能化的膜通道实现区室间的信号传递和通信。
利用多步骤微流控方法,通过双乳液模板的脱湿工艺,可以逐层组装嵌套脂质体结构,形成同心、偏心或多区室的脂质体。
3) 非膜组分的装载
人工细胞非膜组分的装载主要有3种方式:一是在膜上和膜内特定区域组装设定组分。第二种是利用生物或化学等手段,由已有组分产生新组分,如利用无细胞表达系统在内部重建蛋白质生产能力。第三种方式则利用人工细胞的操作手段,如物理穿孔,跨膜运输等实现膜上或膜内成分改变。
4) 其他细胞结构的构建
除了膜结构和内容物的装载外,还需要构建细胞骨架、细胞壁和鞭毛等特征结构。将细胞骨架系统引入人工细胞,可通过渗透调节改变细胞形状和体积,进而实现迁移、有丝分裂等复杂功能。
微水凝胶网络可模拟细胞骨架,增强脂质体对渗透压冲击的抵抗力,并通过固定纳米颗粒进行功能化。
植物细胞的完整性依赖于细胞壁,因此在人工植物细胞中模拟细胞壁结构至关重要。常用材料包括纤维素纳米纤维和果胶,通过果胶与纤维素嵌合蛋白或半纤维素网络结合,模拟细胞壁。鞭毛通过异时运动在自我推进、捕食和细胞运输中发挥关键作用。
5) 非囊泡人工细胞的制备
非囊泡人工细胞的形成主要依赖自组装,通过多尺度协同作用将分子组织成有序结构。这种方法虽然简单快捷,但生成的人工细胞尺寸单分散性较差,生产效率也较低。
微流控技术可以提高自组装过程的精确控制。此外,非囊泡人工细胞的微流控制备还可以通过物理化学聚合实现。在加热或紫外线照射下,液滴可以聚合成固体微粒。
© 2025. All Rights Reserved. 苏ICP备2022036544号-1















