癌症
癌症是21世纪以来对人类身体健康危害最大的疾病之一,全世界每年大概有1000万人死于癌症。
但当前的医疗技术手段还有很大提升空间,首个通过美国食品和药物监督管理局(FDA)的批准的CellSearch系统已经应用在临床CTC检测系统,能够用于多种癌症的疗效监测和预后评估,可以为转移性结直肠癌、乳腺癌和前列腺癌患者的预后提供信息。
但该平台对上皮标志物的依赖和对免疫抗原表达细胞的排除未能捕捉到具有预后价值的重要亚群。
而且由于CellSearch系统的低敏性,它几乎只能用于晚期癌症检测,因此它不能有效地检测癌症的早期和中期进展。
但是特别是对癌症早期患者来说,如果能及时发现并采取治疗干预的话,就是治疗癌症的最佳时期。
CTC
近些年来,科学家们发现了一种新型检测技术——液体活检。
液体活检是一种微创方法,用于检测体液中具有预后或诊断作用的肿瘤衍生标志物,具有早期诊断、转移跟踪、耐药性预测、预后复发监测等特点。
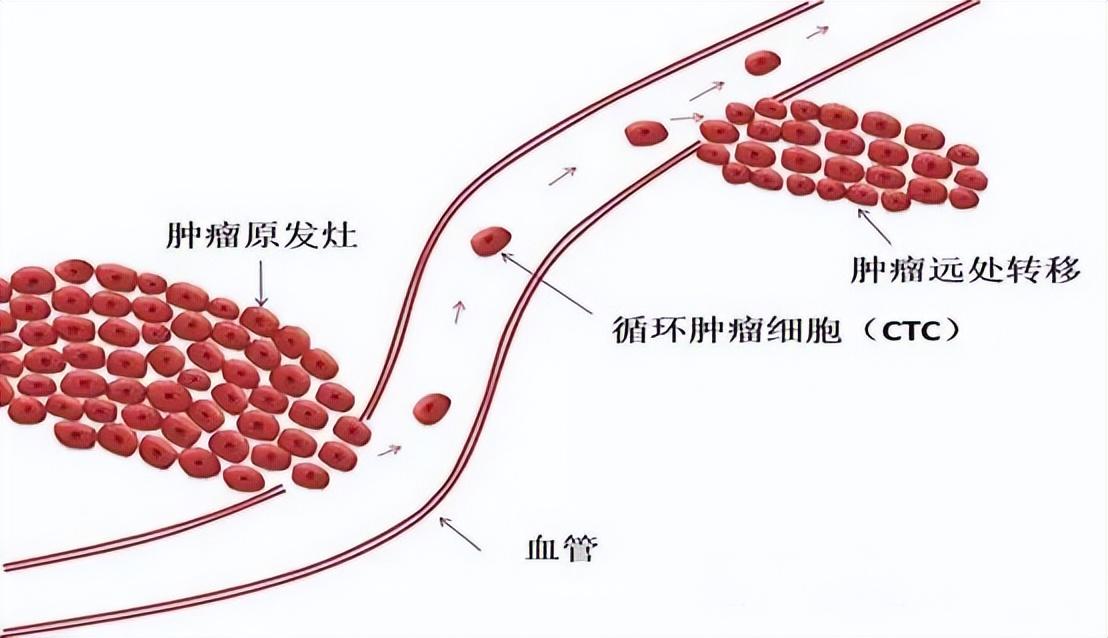
作为液体活检的重要标志物之一,循环肿瘤细胞(CTC)在外周血中的含量可以用来辅助判断患者的癌症病发状况。
除此以外,CTC对于肿瘤细胞转移行为等基础研究也具有非常重要的意义。
然而人体血液中的CTC含量极其稀少,通常仅有0~10个/mL,与之相对,红细胞、白细胞和血小板的含量则分别达到5×109个/mL、4×106个/mL和3×108个/mL,而且肿瘤细胞在转移过程中可以通过上皮⁃间质转化(EMT)和间质⁃上皮转化(MET)来不断地改变自身的特征。
正是由于其稀缺性和异质性,以及血液中复杂基质的干扰,CTC的精准检测成为巨大的难题。
常规检测技术
由于常规的光学分析手段在检出限和灵敏度上均难以达到直接检测的要求,因此通常在进行外周血中CTC的检测之前,要通过一些样品前处理方法来实现其分离和富集。
常采用的样品前处理方法可以分为物理法和化学法。
物理法主要根据细胞在物理特征上的差异来进行分离,例如膜过滤分离和密度梯度离心,就是分别依据细胞的大小和密度来完成筛选。
化学法则主要依靠生物大分子的特异性识别作用,例如抗原抗体相互作用,核酸适配体与靶标的选择性结合。
常规检测技术缺陷
上述样品前处理方法虽然能够在不同程度上实现CTC的分离富集,但也存在着一定的缺陷。
由于这些方法都是非连续性的,在吸附、洗脱和转移的过程中难免会造成细胞的丢失,加之CTC本身的稀缺性,很容易导致假阴性结果的产生。
结合微流控芯片的检测技术
利用微流控芯片功能集成的特点则可以很好地解决这一问题,CTC的捕获、释放、计数及检测等操作均可在芯片上完成,连续的自动化处理可以有效减少人为误差的干扰。
此外,微流控芯片所需要的进样量非常小,可以大大减少珍贵样品和试剂的消耗,降低检测成本。
并且在微尺度下表面力的作用会明显放大,可以有效提高物质混合和反应的效率,实现快速高效的分离分析。
因此,近年来多项研究尝试利用微流控芯片平台开展CTC分离检测工作,取得了良好的效果。
基于物理特性的微流控芯片方法
a)大小和可变形性
基于细胞大小差异筛选出CTC是很早以前就使用的分离方法之一,这种技术方法相对来说比较简单而且成本比较低。
有报道指出一种基于CTC的大小和变形性来实现CTC的富集,并自动染色用于细胞识别,随后从这种微流控芯片出口中回收细胞的微流控芯片。
使用这种微流控芯片,平均细胞捕获效率为42%至70%。最重要的是,使用这种微流控芯片处理患者的样本后回收的CTC存活率高,并且仍然可以用于下游分子分析。
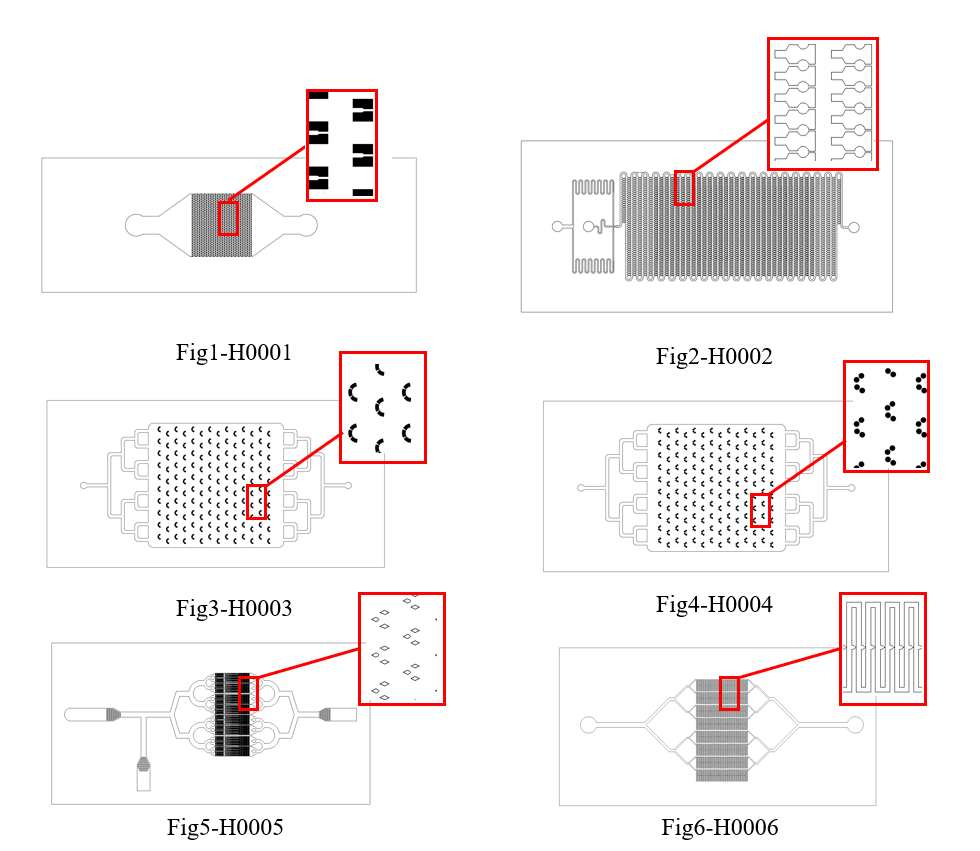
b)流体动力学
据文献报道,通过微流控技术分离循环肿瘤细胞CTC是一种比较高效的方法,主要是将微流控技术与流体力学相结合。
当流体在微通道中流动时,流体中的悬浮细胞与微流控芯片内部发生碰撞,产生一定的作用力,不同尺寸的细胞就会产生不一样的流动轨迹,所以循环肿瘤细胞CTC就可以与血细胞分离。
基于确定性侧向位移芯片(DLD)的分离是一种根据细胞大小和流体动力学结合将CTC和血细胞分离的技术方法。
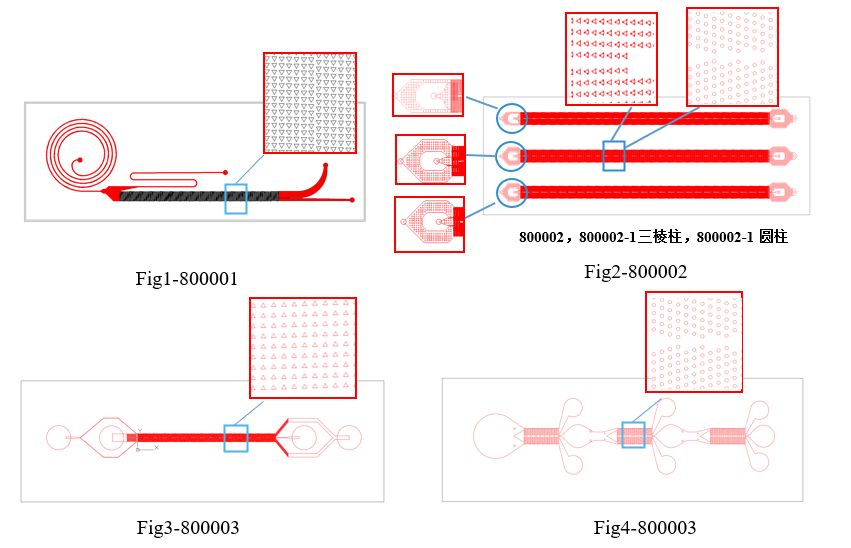
根据DLD的原理,超过设计临界尺寸的大颗粒(如癌细胞)将沿着阵列的倾斜轴流动,而流体和小颗粒将沿着阵列的水平方向流动。
使用这种微流控芯片可以在几分钟内从几毫升的临床血液样本中分离出85%以上的CTC,而且不影响细胞活力,以便对细胞进行下一步的培养和分析。
c)介电电泳
不同细胞因为它们的性质不同,比如直径、膜电容、胞质电导率等不同的物理性质,具有不一样的介电参数。
介电电泳是一种用于细胞与其他分子或者细胞与细胞之间的分离方法。不同性质的细胞在同样的电场作用下产生不同的介电力,由于循环肿瘤细胞CTC与血细胞不一样,所以可以通过介电电泳方法用于CTC与血细胞的分离。
有相关研究设计了一种通过继电器在相邻电极对之间切换电场进而产生步进电场的圆形微电极的微流控芯片,可以有效地从外周血样本中分离宫颈癌细胞(HeLa)。
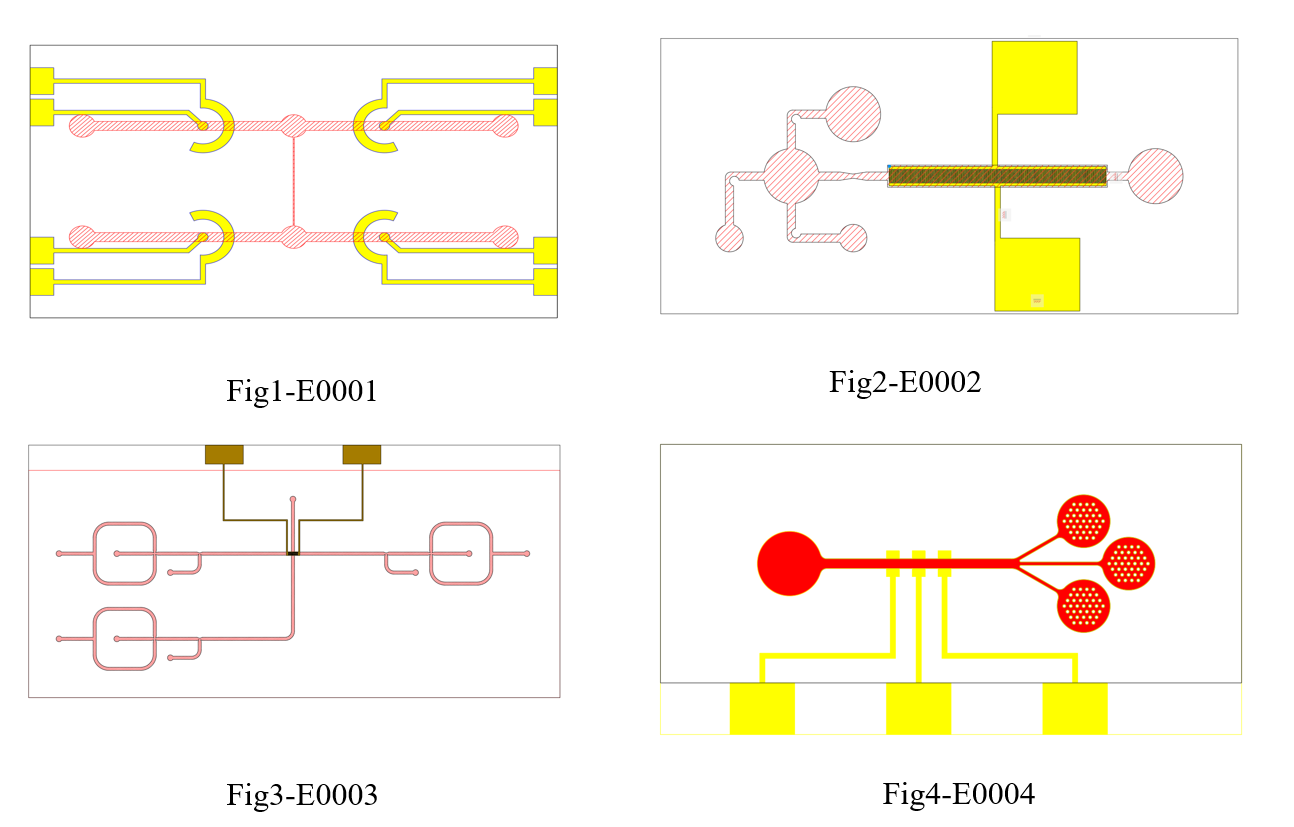
基于化学特性的微流控芯片方法
a)抗体识别
在分离循环肿瘤细胞CTC的技术方法中,基于抗体亲和性的分离方法是CTC分离最常见的方法之一。
上皮细胞黏附分子(EpCAM)在上皮细胞癌变的过程中起作用,是区分CTC与血细胞重要的生物标志物。
通过将EpCAM抗体修饰在微流控芯片的内部结构中,当样本通入微流控芯片内部时,EpCAM抗体会特异性地识别出目标CTC,并与靶标形成非共价键,进而CTC被捕获于微流控芯片当中,其他细胞则随缓冲液流出。
相关报道描述了一种新的微流控芯片(SDI-Chip),用于高效率、高特异性的CTC捕获和检测。
b)核酸适配体识别
核酸适配体是经过体外筛选得到的一小段单链DNA或RNA,它可以与目标配体形成非共价键并特异性地结合。
核酸适配体与靶标的结合主要是通过螺旋折叠的方式与靶配体的互补序列结合,而抗体与靶标的结合主要是与目标抗原表面特异性的抗原簇结合。
有研究指出了一种微流控芯片,使用10纳米以下的三维DNA结构作为框架,顶部修饰了一个适配体。
垂直纳米框架确保了适配体处于高度有序的直立方向,更有利于微流控芯片上的适配体与样本中的CTC接触,并提高CTC的捕获效率。
其他拓展——3D打印微流控芯片
传统的微流控设备基于光刻的制造工艺,复杂的制造步骤、昂贵的材料成本、耗时的制作过程均限制了微流控设备从实验室到实际临床实施的转化。
与之相比,3D打印技术具有相对灵活性、直接性和快速原型制作的能力,能够逐层打印出多种复杂的三维结构,增加了微流控芯片的功能表面积,为精确和小型的微流控芯片制造提供便利。
此外,各种适宜的原材料的出现将不断丰富微流控设备的应用范围,促进其在研究和临床环境中被广泛接受。

3D打印微流控芯片可以为CTC检测和早期监测肿瘤转移开辟新机会,尽管目前关于此类芯片的研究应用不多,但是可以预测,3D打印技术在未来将会成为微流控芯片制造领域最为重要方法之一,为CTC检测广泛应用于临床提供有益的见解。
关于我们
顶旭(苏州)微控技术有限公司是一家专注于微流控领域的高科技企业,我们致力于为客户提供微流控芯片定制、表面修饰改性、微流控芯片加工设备、以及微流控仪器等全面的微流控解决方案。公司团队拥有丰富的经验和技术积累,持续将专业知识与创新思维相结合,为客户提供高品质的解决方案。我们将始终坚持以客户为中心,不断挑战自我,不断追求卓越,通过专业、创新和合作,为客户创造更大的价值,共同开创微流控领域的美好未来。
© 2025. All Rights Reserved. 苏ICP备2022036544号-1















