1. 类器官与器官芯片
类器官是由多能干细胞或成体干细胞生成的三维结构,能够再现人体器官的结构、功能及组织特性,广泛应用于个性化医疗和临床前药物测试。
常见的类器官培养方法包括浸没培养、气-液交互培养和共培养等。
器官芯片(organ-on-a-chip,OOC)是一种微流控技术制造的细胞培养设备,通常由微型灌注腔室构成,具有多层细胞结构、组织界面、物理化学微环境以及类血管循环系统。
它能够模拟人体器官的生理功能,是一种微型细胞培养系统。
器官芯片的工作原理是通过模拟流体剪切力、动态机械应力、浓度梯度等生理条件,再现体内复杂的环境,进而研究细胞、组织和血液的相互作用,并在不同刺激下观察病理生理反应,从而提供更为真实可靠的实验数据。
2. 器官芯片及其应用
1) 呼吸系统器官芯片
肺部的气体交换主要通过肺泡的扩张和收缩来增加气体交换面积,而肺泡作为气体交换的主要部位,也是肺的功能单位。
研究团队开发了一种基于微流控芯片的多功能微装置,能够再现肺泡-毛细血管界面上的气-血屏障结构,并实现其核心功能,具备模拟人体肺基本功能单元的能力。
该装置的工作原理如下:装置的核心由上下两个紧密相连的微通道组成,二者通过一层10μm厚的聚二甲基硅氧烷(PDMS)多孔柔性薄膜隔开。
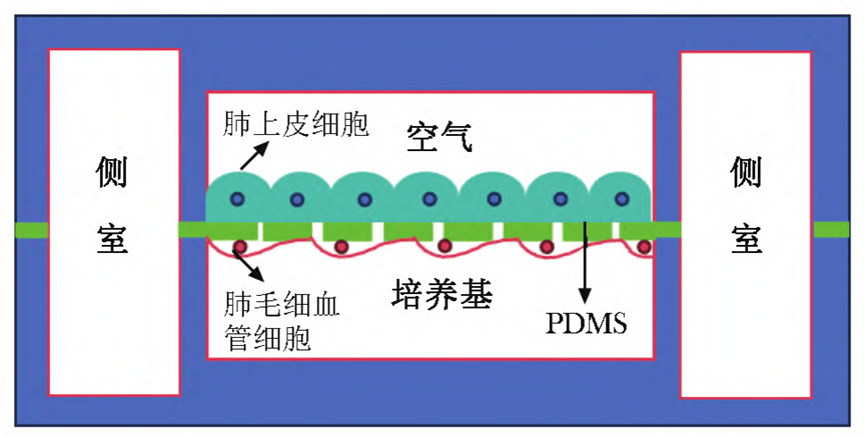
薄膜表面涂覆纤维连接蛋白或胶原蛋白后,上下两面分别培养人肺泡上皮细胞和人微血管内皮细胞。
待细胞生长并汇合后,空气被导入上室,培养基则保留在下室,形成气-液界面。
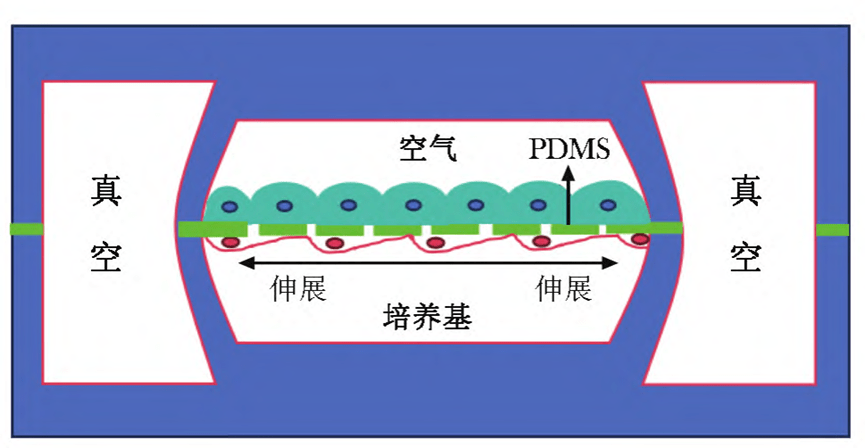
当侧室处于真空状态时,PDMS薄膜发生弹性变形,带动薄膜上的细胞伸展;
当气压恢复时,薄膜的弹性作用使细胞恢复原状,从而模拟呼吸运动引起的肺泡-毛细血管界面的动态力学变化。
2) 循环系统器官芯片
心肌细胞无法再生,药物的心脏毒性在药物评估中至关重要。
为了更好地建立疾病模型并预测药物的心脏毒性,开发更为精准的心脏模型显得尤为关键。
心脏芯片作为一个集可控生理、生化和机械力等多种因素于一体的体外模型,近年来受到广泛关注。
现有的心脏芯片通常由四个主要部分组成:微流控结构、细胞组织与基质、环境控制系统(如氧气梯度、药物输送、机械刺激)以及分析组件(如在线生化传感器和电极)。
这些细胞通常来源于成人供体细胞衍生的诱导多能干细胞,经过培养生成心肌细胞。
基于这一技术,已经开发出多种心脏OOC平台,这些平台通过共培养不同类型的细胞,如心肌细胞、内皮细胞和心脏成纤维细胞,专注于模拟心脏的生物功能。
同时,心脏芯片也广泛用于评估抗癌药物的心脏毒性。
3) 消化系统器官芯片
药物引起的肝损伤是临床前和临床试验中药物失败的主要原因,也是药物上市后撤市的常见原因。
肝器官芯片通常使用原代人肝细胞或细胞系,但随着培养时间的延长,细胞功能会逐渐下降。
为解决这一问题,研究通过与星形胶质细胞、成纤维细胞、内皮细胞的共培养以及血流灌注等方式,能部分恢复肝细胞的功能。
由于肝脏在药物代谢和毒性作用中的独特角色,肝脏芯片常与其他器官芯片结合,成为多器官芯片研究的重点模型。
肠道是人体主要的营养消化、吸收和代谢器官,也是宿主与共生菌群互动以及黏膜免疫的关键区域。
肠器官芯片通过结合微流控技术和模拟力作用,能更真实地再现肠道的解剖和生理结构。
在此基础上,研究者开发了克罗恩病、溃疡性结肠炎等肠道疾病模型,并利用肠器官芯片建立了一系列肠道感染模型,用于研究病原体的致病机制。
4) 神经系统———脑/血脑屏障芯片
人脑的复杂结构和功能,特别是血脑屏障的存在,使得神经系统药物的开发面临独特挑战。
血脑屏障通过选择性控制药物进入中枢神经系统,增加了药效预测的难度。
因此,脑芯片的研发主要聚焦于模拟血脑屏障功能,通过精确的细胞三维排列、细胞间的相互作用,以及器官特有的机械和生化梯度,重建具有生理功能的人类血脑屏障。
这为测试针对神经系统疾病的药物是否能够穿越血脑屏障并在特定靶点发挥作用提供了重要平台。
血脑屏障芯片模型已广泛应用于神经病理学的各类疾病建模,帮助深入理解疾病的发病机制和进程,识别潜在的治疗靶点,并评估新药物的治疗效果。
目前,已建立的疾病模型包括阿尔茨海默病、帕金森病以及神经炎症反应等。
5) 泌尿系统———肾芯片
肾脏在人体的代谢、排泄和重吸收过程中发挥着关键作用,是药物毒性的主要靶器官。
药物引起的肾损伤是评估药物毒性和确定安全剂量的重要因素。
肾近曲小管是最易受到药物毒性影响的部位,因此,近端小管OOC模型在药物毒性预测中具有重要意义。
部分器官芯片在药物毒性测试中的准确性优于传统的临床前模型。
因此,研究人员可以对一些未通过临床前试验的药物重新进行毒性评估,这可能带来新的发现。
此外,肝脏和肾脏作为身体的主要解毒器官,它们之间存在紧密的相互作用。
肝-肾器官芯片的建立及其药物代谢数据表明,多器官协同作用平台相比单一器官芯片能更敏感地反映药物的毒性反应,这使得它们在替代动物模型进行药物毒性筛选时展现出更高的潜力。
6) 其他芯片
随着器官芯片技术的不断进步,研究者对器官芯片的种类和功能提出了更高的要求。
皮肤芯片、骨芯片、肌肉芯片、视网膜芯片以及肿瘤芯片等相继问世,为构建更贴近人体生理和病理状态的器官芯片平台及多器官芯片联合平台奠定了基础。
在此基础上,将肿瘤芯片与其他器官芯片联合,能够更系统地研究肿瘤如何通过血管和淋巴管进行侵袭和转移等复杂的病理过程及生理反应。
随着单个器官芯片功能的逐步完善,当这些芯片具备了模拟相应器官的关键特征后,它们可以被组合成一个多器官芯片联合平台,这种平台也可被称为人体芯片。
通过微流控技术模拟血管灌注等体内环境,将不同的单器官芯片互联,能够再现器官之间复杂的动态相互作用,提供更接近生理状态的药物传递、分布和吸收模型。
© 2025. All Rights Reserved. 苏ICP备2022036544号-1















